Номер 11, страница 86 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 2. Важнейшие классы неорганических соединений. Параграф 20. Основания - номер 11, страница 86.
№11 (с. 86)
Условие. №11 (с. 86)
скриншот условия

11. Рассчитайте массу гидроксида магния, который нужно добавить к гидроксиду кальция массой 14,8 г, чтобы общее химическое количество оснований в смеси было равно 0,45 моль.
Решение. №11 (с. 86)
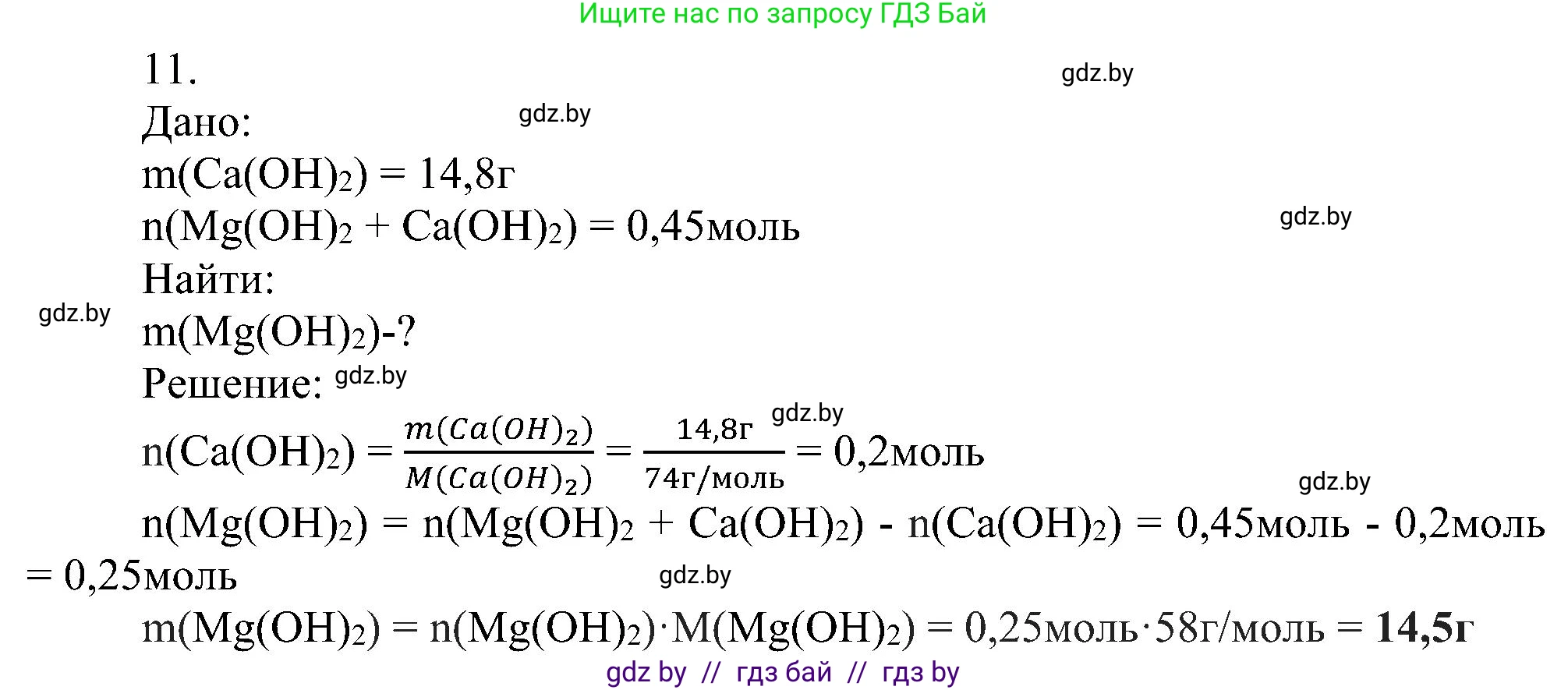
Решение 2. №11 (с. 86)
Дано:
Масса гидроксида кальция $m(Ca(OH)_2) = 14,8 \text{ г}$
Общее химическое количество оснований в смеси $n_{общ} = 0,45 \text{ моль}$
Найти:
Массу гидроксида магния $m(Mg(OH)_2)$
Решение:
1. Сначала определим химическое количество ($n$) гидроксида кальция $Ca(OH)_2$, имеющегося в наличии. Для этого нам понадобится его молярная масса ($M$).
Молярная масса гидроксида кальция $M(Ca(OH)_2)$ рассчитывается на основе относительных атомных масс элементов: $Ar(Ca) = 40$, $Ar(O) = 16$, $Ar(H) = 1$. $M(Ca(OH)_2) = Ar(Ca) + 2 \cdot (Ar(O) + Ar(H)) = 40 + 2 \cdot (16 + 1) = 40 + 34 = 74 \text{ г/моль}$
Теперь найдем химическое количество гидроксида кальция по формуле $n = \frac{m}{M}$: $n(Ca(OH)_2) = \frac{14,8 \text{ г}}{74 \text{ г/моль}} = 0,2 \text{ моль}$
2. Общее химическое количество оснований в смеси является суммой химических количеств гидроксида кальция и гидроксида магния: $n_{общ} = n(Ca(OH)_2) + n(Mg(OH)_2)$
Из этого уравнения мы можем найти необходимое химическое количество гидроксида магния $Mg(OH)_2$: $n(Mg(OH)_2) = n_{общ} - n(Ca(OH)_2) = 0,45 \text{ моль} - 0,2 \text{ моль} = 0,25 \text{ моль}$
3. Чтобы найти массу гидроксида магния, нам нужна его молярная масса $M(Mg(OH)_2)$. Рассчитаем ее, используя относительные атомные массы: $Ar(Mg) = 24$, $Ar(O) = 16$, $Ar(H) = 1$. $M(Mg(OH)_2) = Ar(Mg) + 2 \cdot (Ar(O) + Ar(H)) = 24 + 2 \cdot (16 + 1) = 24 + 34 = 58 \text{ г/моль}$
4. Наконец, рассчитаем массу гидроксида магния по формуле $m = n \cdot M$: $m(Mg(OH)_2) = n(Mg(OH)_2) \cdot M(Mg(OH)_2) = 0,25 \text{ моль} \cdot 58 \text{ г/моль} = 14,5 \text{ г}$
Ответ: необходимо добавить 14,5 г гидроксида магния.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 11 расположенного на странице 86 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №11 (с. 86), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













