Номер 8, страница 140 - гдз по химии 8 класс учебник Шиманович, Красицкий

Авторы: Шиманович И. Е., Красицкий В. А., Сечко О. И., Хвалюк В. Н.
Тип: Учебник
Издательство: Адукацыя i выхаванне
Год издания: 2024 - 2025
Цвет обложки: синий, розовый с таблицей Менделеева
ISBN: 978-985-03-2941-7
Допущено Министерством образования Республики Беларусь
Популярные ГДЗ в 8 классе
Глава 3. Периодический закон и периодическая система химических элементов. Параграф 32. Периодическая система химических элементов - номер 8, страница 140.
№8 (с. 140)
Условие. №8 (с. 140)
скриншот условия
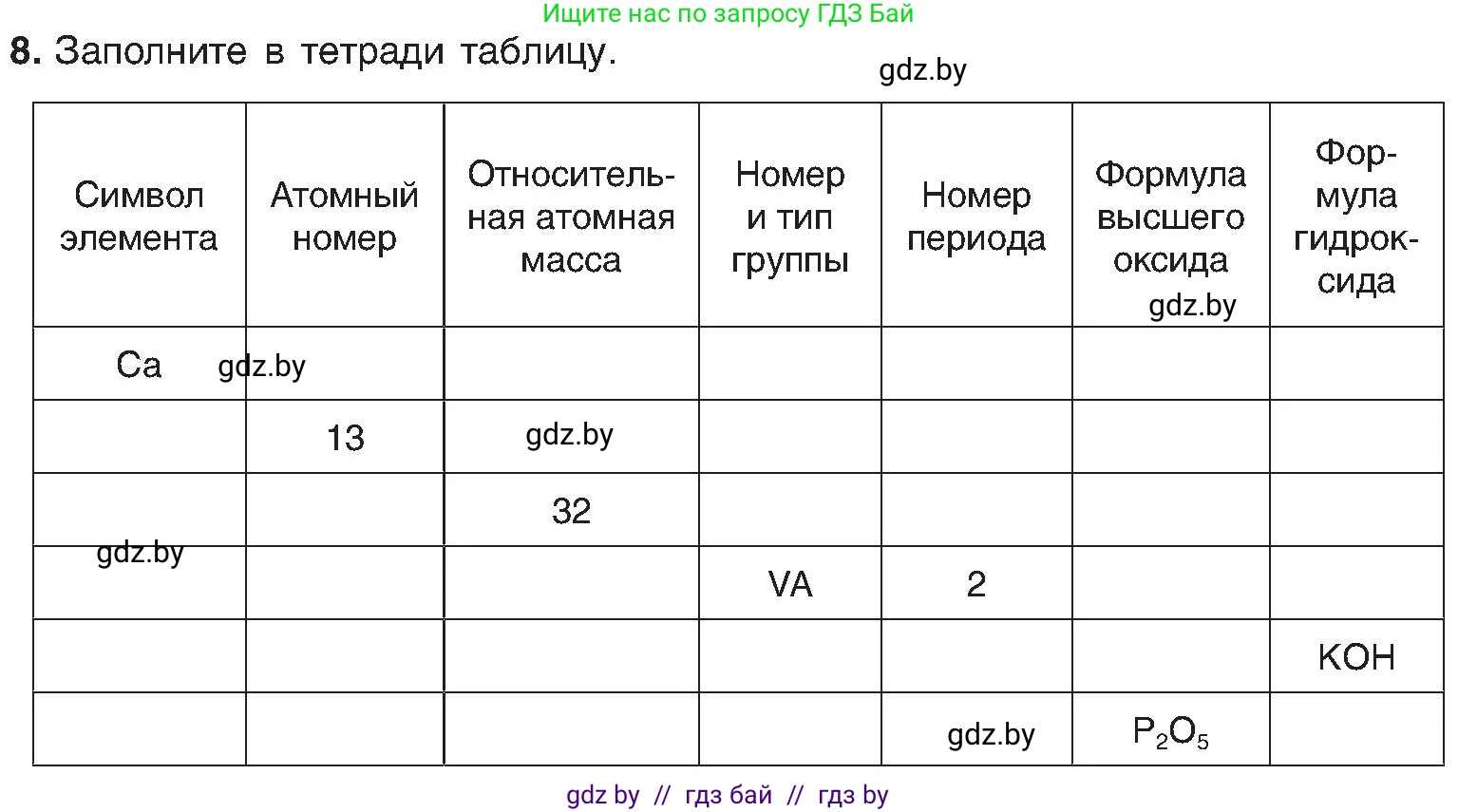
8. Заполните в тетради таблицу.
| Символ элемента | Атомный номер | Относительная атомная масса | Номер и тип группы | Номер периода | Формула высшего оксида | Формула гидроксида |
| $Ca$ | ||||||
| 13 | ||||||
| 32 | ||||||
| VA | 2 | |||||
| KOH | ||||||
| ${P}_{2}{O}_{5}$ |
Решение. №8 (с. 140)

Решение 2. №8 (с. 140)
Ниже представлено развернутое решение для заполнения каждой строки таблицы.
CaДано:
Символ элемента: Ca (Кальций)
Найти:
Атомный номер, Относительная атомная масса, Номер и тип группы, Номер периода, Формула высшего оксида, Формула гидроксида.
Решение:
Используя Периодическую систему химических элементов Д. И. Менделеева, находим элемент Кальций (Ca).
1. Атомный номер (порядковый номер) кальция — 20.
2. Относительная атомная масса элемента равна 40,078. Округляем до целого числа — 40.
3. Кальций находится во второй группе ($II$), главной подгруппе (A). Тип группы — $IIA$.
4. Кальций расположен в четвертом периоде.
5. Высшая валентность элемента главной подгруппы равна номеру группы, то есть $II$. Степень окисления в высшем оксиде $+2$. Формула высшего оксида, где степень окисления кислорода $-2$, будет $CaO$.
6. Оксид кальция $CaO$ является основным оксидом, ему соответствует основание (гидроксид) — гидроксид кальция, формула которого $Ca(OH)_2$.
Ответ: Ca, 20, 40, IIA, 4, $CaO$, $Ca(OH)_2$.
13Дано:
Атомный номер: 13
Найти:
Символ элемента, Относительная атомная масса, Номер и тип группы, Номер периода, Формула высшего оксида, Формула гидроксида.
Решение:
1. Элемент с атомным номером 13 — это Алюминий, символ $Al$.
2. Относительная атомная масса алюминия равна 26,982. Округляем до целого числа — 27.
3. Алюминий находится в третьей группе ($III$), главной подгруппе (A). Тип группы — $IIIA$.
4. Алюминий расположен в третьем периоде.
5. Высшая валентность алюминия равна $III$, степень окисления $+3$. Формула высшего оксида: $Al_2O_3$.
6. Оксид алюминия $Al_2O_3$ является амфотерным оксидом, ему соответствует амфотерный гидроксид — гидроксид алюминия, формула которого $Al(OH)_3$.
Ответ: Al, 13, 27, IIIA, 3, $Al_2O_3$, $Al(OH)_3$.
32Дано:
Относительная атомная масса: 32
Найти:
Символ элемента, Атомный номер, Номер и тип группы, Номер периода, Формула высшего оксида, Формула гидроксида.
Решение:
1. Находим в периодической таблице элемент с относительной атомной массой, близкой к 32. Это Сера (S), её масса 32,065.
2. Атомный номер серы — 16.
3. Сера находится в шестой группе ($VI$), главной подгруппе (A). Тип группы — $VIA$.
4. Сера расположена в третьем периоде.
5. Высшая валентность серы равна $VI$, степень окисления $+6$. Формула высшего оксида: $SO_3$.
6. Оксид серы(VI) $SO_3$ является кислотным оксидом, ему соответствует кислота (гидроксид) — серная кислота, формула которой $H_2SO_4$.
Ответ: S, 16, 32, VIA, 3, $SO_3$, $H_2SO_4$.
VA, 2Дано:
Номер и тип группы: VA, Номер периода: 2
Найти:
Символ элемента, Атомный номер, Относительная атомная масса, Формула высшего оксида, Формула гидроксида.
Решение:
1. Находим элемент, расположенный на пересечении второго периода и пятой группы ($V$), главной подгруппы (A). Это Азот, символ $N$.
2. Атомный номер азота — 7.
3. Относительная атомная масса азота равна 14,007. Округляем до целого числа — 14.
4. Высшая валентность азота равна $V$, степень окисления $+5$. Формула высшего оксида: $N_2O_5$.
5. Оксид азота(V) $N_2O_5$ является кислотным оксидом, ему соответствует кислота (гидроксид) — азотная кислота, формула которой $HNO_3$.
Ответ: N, 7, 14, VA, 2, $N_2O_5$, $HNO_3$.
KOHДано:
Формула гидроксида: $KOH$
Найти:
Символ элемента, Атомный номер, Относительная атомная масса, Номер и тип группы, Номер периода, Формула высшего оксида.
Решение:
1. $KOH$ — это гидроксид калия. Следовательно, искомый элемент — Калий, символ $K$.
2. Атомный номер калия — 19.
3. Относительная атомная масса калия равна 39,098. Округляем до целого числа — 39.
4. В соединении $KOH$ калий проявляет степень окисления $+1$. Элементы с высшей степенью окисления $+1$ находятся в первой группе ($I$), главной подгруппе (A). Тип группы — $IA$.
5. Калий расположен в четвертом периоде.
6. Высшему гидроксиду $KOH$ соответствует высший оксид $K_2O$.
Ответ: K, 19, 39, IA, 4, $K_2O$, $KOH$.
P₂O₅Дано:
Формула высшего оксида: $P_2O_5$
Найти:
Символ элемента, Атомный номер, Относительная атомная масса, Номер и тип группы, Номер периода, Формула гидроксида.
Решение:
1. Элемент в оксиде $P_2O_5$ — это Фосфор, символ $P$.
2. Определим степень окисления фосфора в данном оксиде. Пусть она равна $x$. Тогда $2x + 5 \cdot (-2) = 0$, откуда $2x = 10$ и $x = +5$. Высшая степень окисления $+5$ характерна для элементов пятой группы ($V$), главной подгруппы (A). Тип группы — $VA$.
3. Находим фосфор в V группе периодической таблицы. Его атомный номер — 15.
4. Относительная атомная масса фосфора равна 30,974. Округляем до целого числа — 31.
5. Фосфор расположен в третьем периоде.
6. Высшему оксиду фосфора $P_2O_5$ (кислотный оксид) соответствует ортофосфорная кислота (гидроксид), формула которой $H_3PO_4$.
Ответ: P, 15, 31, VA, 3, $P_2O_5$, $H_3PO_4$.
Другие задания:
Помогло решение? Оставьте отзыв в комментариях ниже.
Присоединяйтесь к Телеграм-группе @gdz_by_belarus
ПрисоединитьсяМы подготовили для вас ответ c подробным объяснением домашего задания по химии за 8 класс, для упражнения номер 8 расположенного на странице 140 к учебнику 2024 года издания для учащихся школ и гимназий.
Теперь на нашем сайте ГДЗ.ТОП вы всегда легко и бесплатно найдёте условие с правильным ответом на вопрос «Как решить ДЗ» и «Как сделать» задание по химии к упражнению №8 (с. 140), авторов: Шиманович (Игорь Евгеньевич), Красицкий (Василий Анатольевич), Сечко (Ольга Ивановна), Хвалюк (Виктор Николаевич), учебного пособия издательства Адукацыя i выхаванне.













